

中国卒中学会第五届学术年会暨天坛国际脑血管病会议,2019于6月28日-6月30日,在北京国家会议中心隆重召开。
中国是卒中大国,卒中所带来的疾病负担日益加重,来自2016年全球疾病负担研究(GBD)数据显示,全球1,370万人新发生卒中,中国占到40%;全球550万人因卒中死亡,中国占1/3;全球卒中所致伤残调整生命年(DALY)为1.164亿,中国占1/3。从数据中我们会发现,中国的卒中,特别是缺血性卒中患病率仍高居心脑血管疾病的首位。为避免卒中大发生,其一、二级预防对于疾病的发展及长期管理十分关键,此次会议上众多医学教授讲解关于卒中危险因素预防与控制进展。我们节选了部分精彩报告与大家分享。

《一级预防抗凝治疗对心源性卒中患者侧支循环和预后的影响》
四川大学华西医院 何俐教授

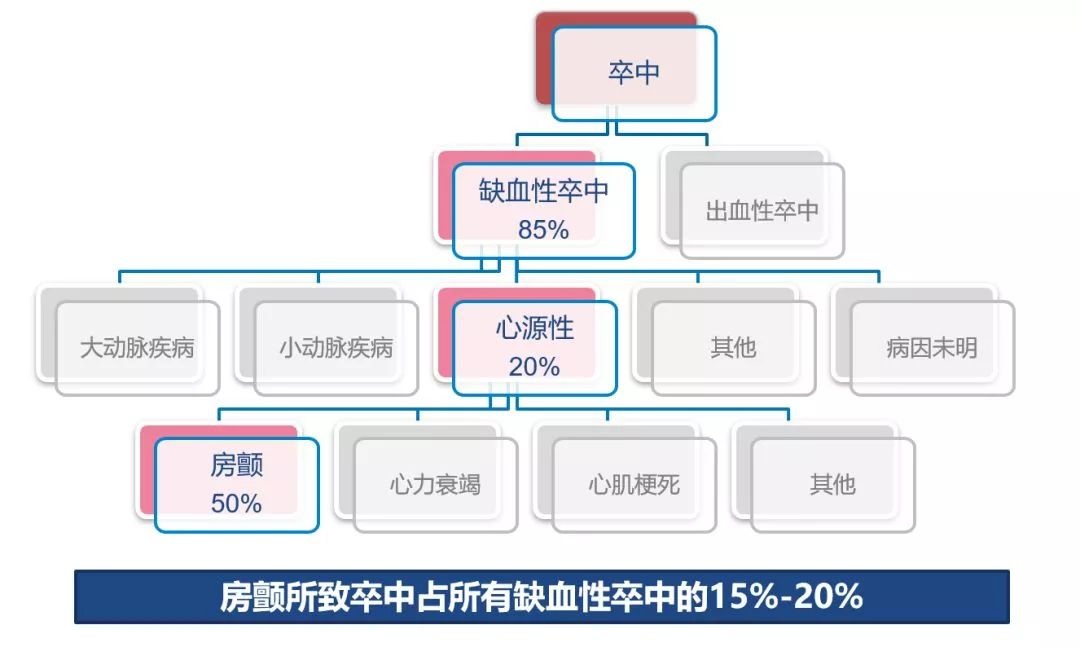
卒中病因分型—TOAST 分型显示:房颤是导致缺血性卒中的重要病因,房颤所致卒中占所有缺血性卒中的15%-20%。在临床中,相比非心源性卒中,心源性卒中患者入院时神经功能缺损更严重,且出院时及发病6个月后预后也更差。因此,必须加强一级预防。
《2018 EHRA实践指导:房颤患者应用非维生素K拮抗剂口服抗凝药》强调房颤患者卒中预防应首选新型口服抗凝药(NOAC),而非维生素K拮抗剂(VKA),并对NOAC的禁忌症及适应症进行了相应的推荐:
NOAC禁用于机械人工瓣膜或中到重度二尖瓣狭窄(通常是风湿性的)的房颤患者;
尽管生物瓣膜、二尖瓣修复或经导管主动脉瓣置换术的相关数据有限,但这些患者使用NOAC是可以接受的。肥厚性心肌病患者使用NOAC的经验有限,但从病理生理学角度,这些患者是可以使用该类药物的。
《心源性卒中的病因分析及临床策略》
北京天坛医院 付强教授

在我国,卒中已经成为致死致残的首位原因,其中,心源性卒中是指各种原因所致心脏内附壁血栓脱落,随血流进入脑动脉而阻塞血管,引起该动脉供血区脑组织缺血坏死,而出现局灶性神经功能缺损。
心源性卒中的致病原因有房颤、心肌梗死、心脏瓣膜病、先天性心脏病、心脏粘液瘤、心肌疾病等。临床上应加强卒中的病因筛查,提高心源性卒中的诊断水平。
房颤是临床最常见的心律失常,其发生率是所有其他心律失常总和的2倍,随着年龄的增加,80岁后房颤的发生率高达30%。房颤患者卒中风险升高5倍、心衰风险升高3倍、痴呆风险、死亡率和住院时间均增加2倍。
心源性卒中治疗时应针对病因给予合理的、个体化的干预,包括抗凝治疗,介入封堵或外科手术,预防心源性卒中的复发。
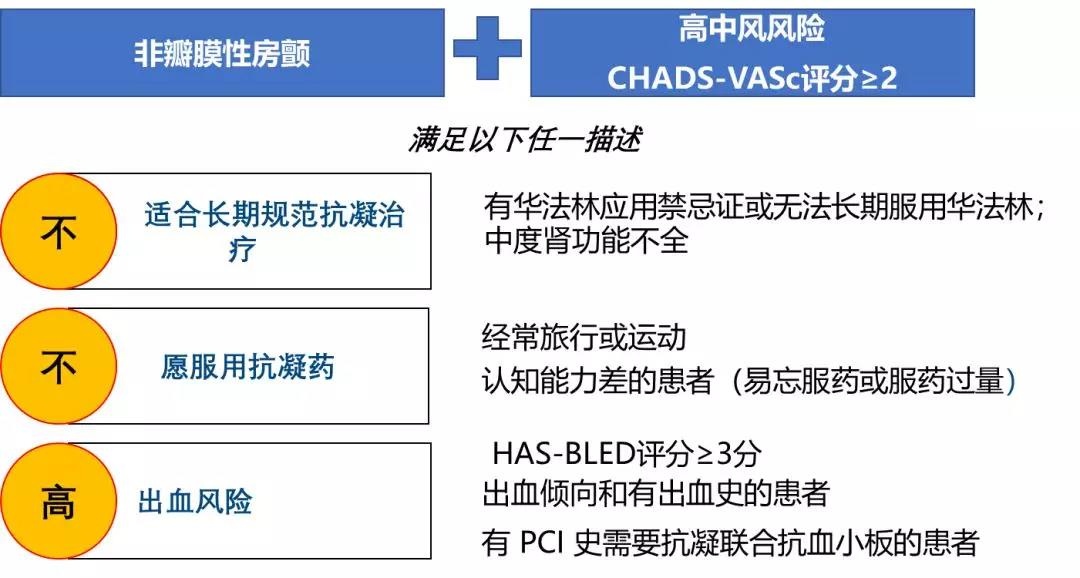
左心耳封堵术适应症
2015中国房颤指南已将左心耳封堵术列为Ⅱa类适应症,上图为左心耳封堵术的适应症。左心耳封堵可以有效降低卒中风险,且无需终身抗凝,无需担心用药出血,一次性解决房颤患者的血栓管理难题。

《从最新指南看卒中二级预防降脂治疗策略》
郑州第一医院 许予明教授

血脂管理是缺血性卒中二级预防的三大基石之一。近年来,随着循证证据的不断丰富,指南也在不断更新。2018年,美国心脏学会(AHA)/美国心脏病学会(ACC)发布最新版胆固醇管理指南(以下简称“2018胆固醇指南”),这是时隔5年,AHA/ACC再次发布的胆固醇管理指南。2018胆固醇指南主要有三大亮点:强调高胆固醇与动脉粥样硬化性心血管疾病(ASCVD)密切相关、肯定了低密度脂蛋白胆固醇(LDL-C)降低带来的临床获益、他汀仍是降脂治疗的基石,非他汀类药物可作为降脂治疗的重要补充。
2018胆固醇指南聚焦ASCVD一级预防和二级预防(本文主要介绍二级预防),并就 “极高风险ASCVD”患者群给出了明确定义。极高风险ASCVD患者包括多个严重ASCVD事件史或1次严重ASCVD事件史合并多个高危因素,详见下图。
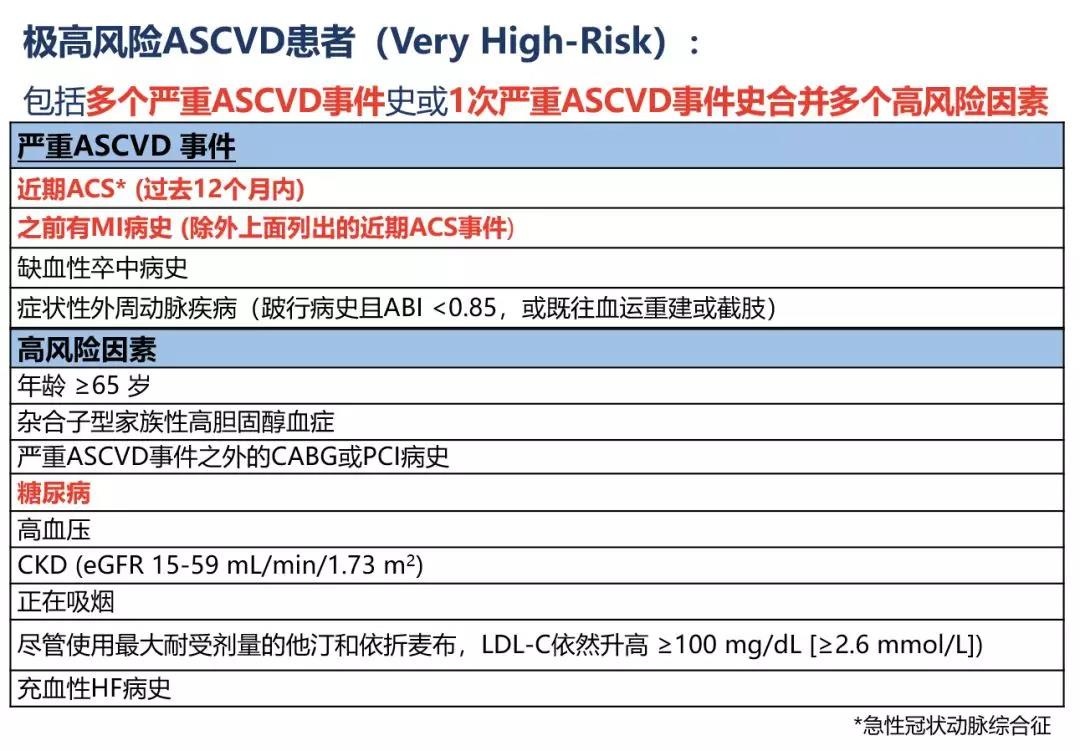
极高危风险ASCVD患者群定义
他汀类药物是重要的降脂药物,2018胆固醇指南就有关他汀类药物使用给予明确建议。2018胆固醇指南强调除生活方式干预外,在调脂治疗中,他汀类药物是治疗的基石。他汀类药物在缺血性卒中二级预防占用稳固地位,这得益于其强力循证医学证据支持。SPARCL研究是目前唯一针对缺血性卒中二级预防的随机对照试验(RCT)。该试验证实高强度他汀治疗一年即可降低卒中复发,高强度他汀治疗5年,可显著降低非心源性缺血性卒中/短暂性脑缺血发作(TIA)患者心血管事件,其中包括致死性或非致死性卒中风险下降16%(p=0.03);卒中/TIA风险下降23%(p<0.001);包括心源性死亡、非致死性心肌梗死、心脏骤停后的复苏、冠状动脉血管重建术、不稳定心绞痛、需急诊住院的心绞痛或心肌缺血在内的任何冠脉事件风险下降42%(p<0.001);非致死性心肌梗死下降49%(p<0.001)。
CTT荟萃分析再次证实高强度他汀治疗可带来更多心脑获益。CTT荟萃分析入选5项高强度他汀对比中等强度他汀治疗的研究(39,612例患者,中位随访5.1年)和21项他汀对比对照组的研究(129,526例患者,中位随访4.8年)。结果显示,对比中等强度他汀,高强度他汀治疗可显著降低主要血管事件风险15%(p<0.0001);冠脉死亡或非致死性心肌梗死风险下降13%(p<0.0001);冠脉血运重建风险下降19%(p<0.0001);缺血性卒中风险下降16%(p<0.0001)。
依折麦布和前蛋白转化酶枯草溶菌素9(PCSK9)抑制剂是两类重要的非他汀类调脂药物,可作为降脂治疗的重要补充。2018胆固醇指南推荐,对于极高风险的ASCVD患者,如果高强度他汀治疗后LDL-C≥1.8mmo/L ,推荐联合非他汀类药物治疗(依折麦布和PCSK9抑制剂)(详见下图红色圈标注)。关于ASCVD患者调脂治疗路径详见下图。
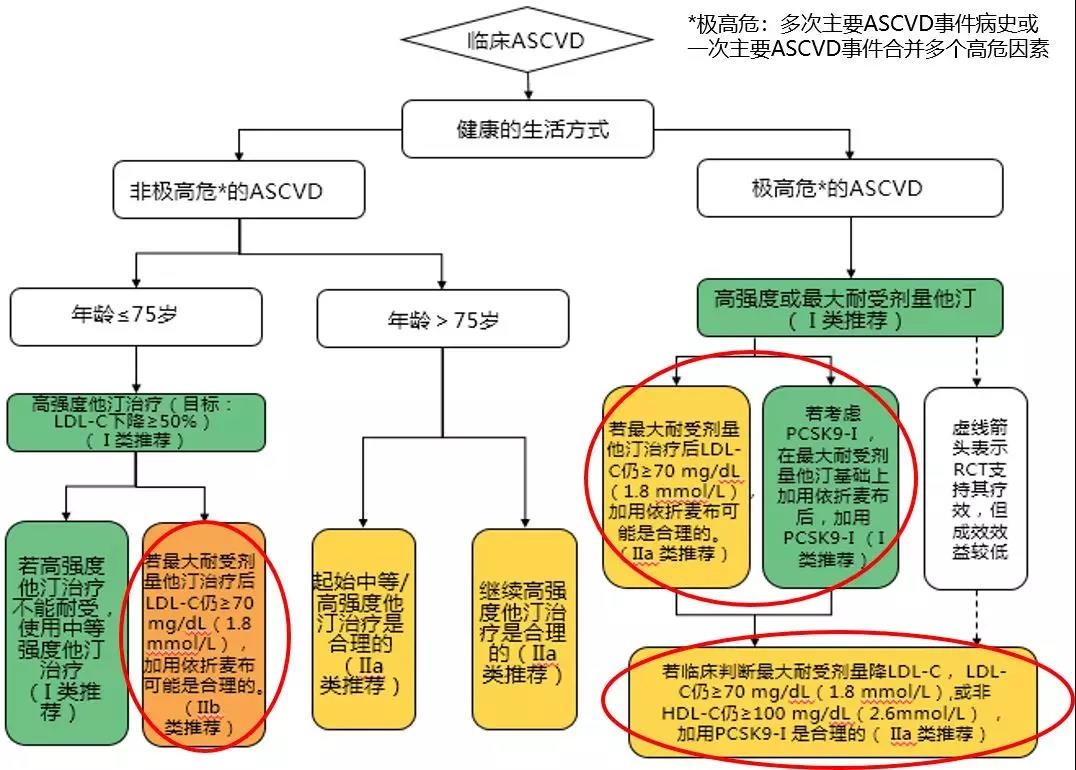
临床ASCVD调脂治疗路径图
2018胆固醇指南聚焦ASCVD防治,再次肯定了他汀类药物的一线基石地位,同时,非他汀类药物可作为降脂治疗的重要补充,这为包括缺血性卒中在内的ASCVD的规范管理提供重要参考。
《卒中后癫痫管理要点》
同济医院 王芙蓉教授

卒中后癫痫(post-stroke epilepsy,PSE)是指卒中前无癫痫病史,在卒中后一定时间内出现癫痫发作,并排除脑部结构和代谢性疾病,脑电图检查与病变部位具有一致性。
根据首次癫痫在卒中后出现的时间点,卒中后痫性发作(post-stroke seizure, PSS )可分为早发性痫性发作(early seizure, ES)和迟发性痫性发作(late seizure, LS)两类。ES的高峰期为卒中后24h内,约45% ES出现于卒中后24h内;LS高峰期为卒中后6~12个月,且有90%的患者会复发。
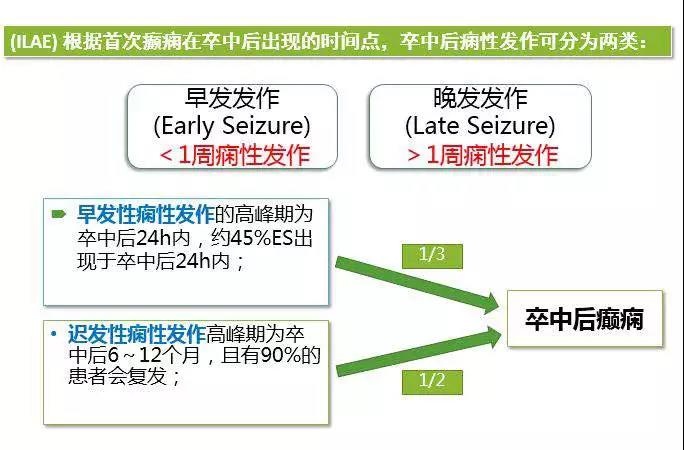
ES可能是继发于局灶性代谢紊乱和兴奋毒性神经递质产生,可能是自限性的;LS可能是由于胶质细胞增生和脑膜脑内瘢痕形成,是持续性的。不同的病理基础造成了早发和晚发的危险因素、再发率、预后、治疗上的不同。
PSE通常被认为是卒中至少1周后发生2次及以上非诱发性痫性发作,通常卒中前无痫性发作的病史,同时排除脑部病变和其他代谢性疾病。卒中后首次非诱发性发作(>1周)10年内再发风险为71.5%(95% CI=59.7-81.9%);根据国际抗癫痫联盟(ILAE)的癫痫新定义,晚发型发作一次也可诊断癫痫。
不同的流行病学调查对PSE的发生率报告不同,发生率在2%~15%范围内。研究显示,年纪轻、起病时严重程度、病灶大小、脑内出血和早期癫痫是卒中后癫痫的独立危险因素。
PSE本质是症状性癫痫,以部分性发作为主要类型,应根据发作类型选择抗癫痫药物(AED)治疗。对于ES发作反复出现或脑出血、蛛网膜下腔出血后的一次癫痫发作,可进行短期AED治疗(3~6月)。单次早发发作,是否采取治疗尚存争议。可以考虑先进行AED治疗,出院时进行 EEG 评估,如无痫性放电,患者再发痫性发作风险较低,则可停药。对于LS,推荐给予长程的AED治疗。多次早发发作或一次迟发发作均需立即给予AED治疗,不推荐预防性AED治疗。
《脑卒中院前与急诊一体化救治》
北京急救中心 李斗教授

李斗教授指出,我国脑卒中院前延误普遍而严重。院前延误原因主要原因:
患者不能早期识别症状
患者未及时就医,观察等待
未使用院前急救(EMS)作为转运途径
EMS到达慢:路途遥远、交通拥堵、急救资源不足
首诊医院无能力,二次转运耽误时间
尤其在急救车使用率方面,我国与欧美国家差距显著:
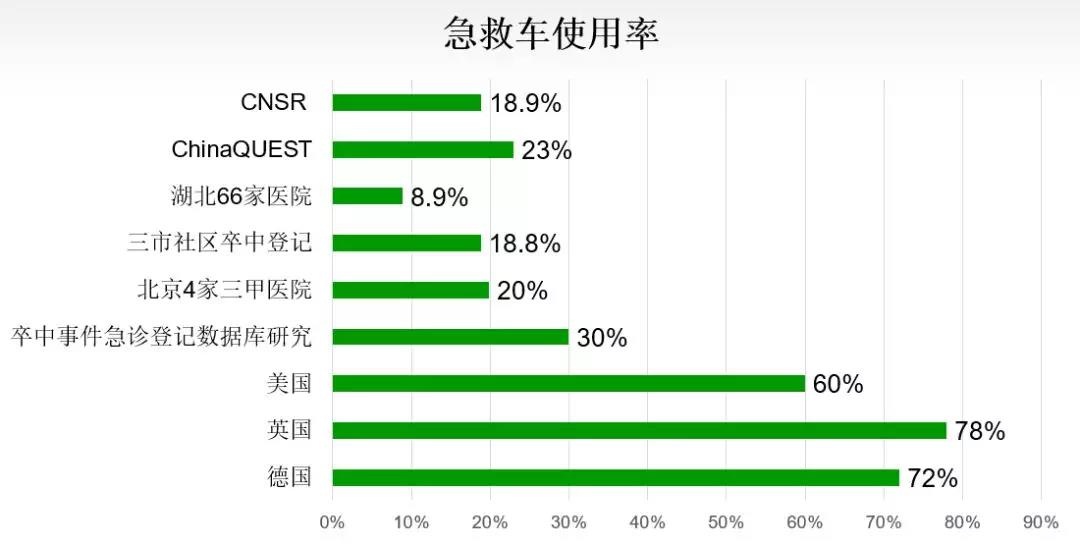
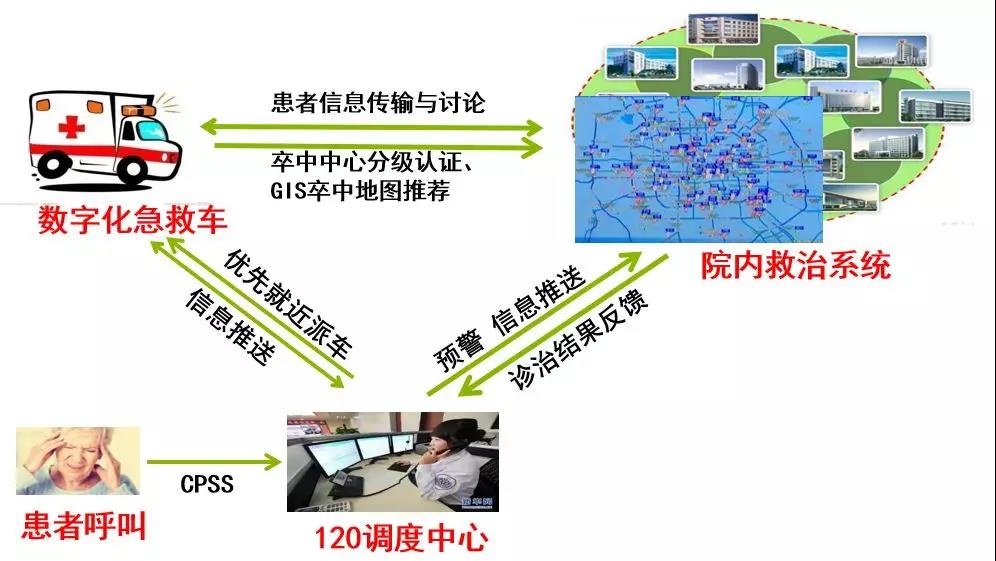
对于脑卒中患者来说,“时间就是大脑”,加强院前院内紧密衔接一体化救治,缩短急救时间,可以使更多患者得到更好治疗,有更好的预后。

以上内容摘自“天坛会”
为了避免卒中的发生,请危险人群及其亲属尽快联系我们,及时进行筛查,进而能够有效的开展诊疗。
